Monday, 12 January, 2026г.
















Где искать: по сайтам Запорожской области, статьи, видео ролики
пример: покупка автомобиля в Запорожье
Estructura Atómica Y Modelos Atómicos - Química-atomo de Bohr
TEORÍAS Y MODELOS ATÓMICOS
Modelo atómico actual
Según el modelo atómico actual el átomo presenta
dos partes: el núcleo y la zona extranuclear.
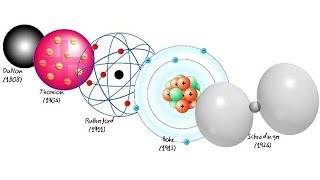
A. Teoría atómica de Dalton (1808)
Su modelo atómico se basa en los postulados que
se presentan a continuación:
1. Todos los elementos químicos están constituidos
por átomos los cuales son partículas invisibles e
indivisibles.
2. Los átomos de un mismo elemento presentan
igual tamaño, masa y otras propiedades.
3. Los átomos diferentes poseen propiedades
diferentes.
4. En una reacción química los átomos se
reordenan sin destruirse, lo cual ocurre en
proporciones numéricas simples.
Modelo atómico de Thomson (1904)
Thomson partiendo de su descubrimiento o plantea
que el átomo es una esfera de masa compacta y
de carga positiva distribuida homogeneamente en
la cual se encuentran incrustados los electrones de
carga negativa de tal manera que neutraliza la carga
positiva de la esfera.
Modelo atómico de Rutherford (1911)
Después de realizar el experimento del pan de oro
Rutherford descubre el núcleo atómico con lo cual
plantea su modelo atómico, que considera al átomo
como un sistema planetario en miniatura cuya parte
central posee un núcleo diminuto y positivo
alrededor del cual giran los electrones en orbitas
circulares y concéntricas.
Modelo atómico de Niels Bohr
Niels Bohr no descarta totalmente el modelo de
Rutherford, estando su modelo basado en los
siguientes postulados.
Primer postulado
Los electrones giran alrededor del núcleo en estado
de equilibrio debido a que las fuerzas que actúan
sobre el se anulan entre si.
Segundo postulado
Los electrones solo pueden girar en ciertas regiones
llamadas niveles de energía.
Tercer postulado
Cuando un electrón gira en un nivel u orbita
permitida no emite ni absorbe energía.
Cuarto postulado
El electrón emite energía cuando se acerca al
núcleo y absorbe energía cuando se aleja de él.
Похожие видео
Мой аккаунт


 У вашего броузера проблема в совместимости с HTML5
У вашего броузера проблема в совместимости с HTML5


